zurück
Home |
Anaplastisches Astrozytom |
Allgemeines |
hochmalignes Gliom |
| Inzidenz |
Bei Erwachsenen 0,3/100.000 EW*a, 4% aller ZNS-Malignome |
| Risikofaktoren |
Neurofibromatose 1 und 2, Tuberöse Sklerose, Li-Fraumeni-Syndrom |
| Prognose |
- 44% 1a-OS
- 16% 3a-OS
- 16% 5a-OS
|
- beste Prognose: 1p/19q Co-Deletion status und IDH - Mutation
- intermediär: IDH - Mutation ohne 1p/19q Co-Deletion
- schlechte Prognose: IDH - Wildtyp
|
| Gen-Analyse (2) |
Astrozytom Grad II:
- TP53-Mutation: 69%
- PDGF/PDGFDR Überexpression
|
Astrozytom Grad III:
- TP53-Mutation: 53%
- PDGF/PDGFDR Überexpression
|
sekundäres Glioblastom:
- LOH 10q: 63%
- EGFR-Amplifikation 8%
- p16INKa4-Deletion 19%
- TP53-Mutation: 65%
- PDGF/PDGFDR Überexpression
- PTEN - Mutation: 5%
|
| Myelon |
63-jähriger Mann mit Querschnittssymptomatik. Auch nach Dekompression keine Motorik oder Sensorik der unteren Körperhälfte. |
MRT T1W-Bild
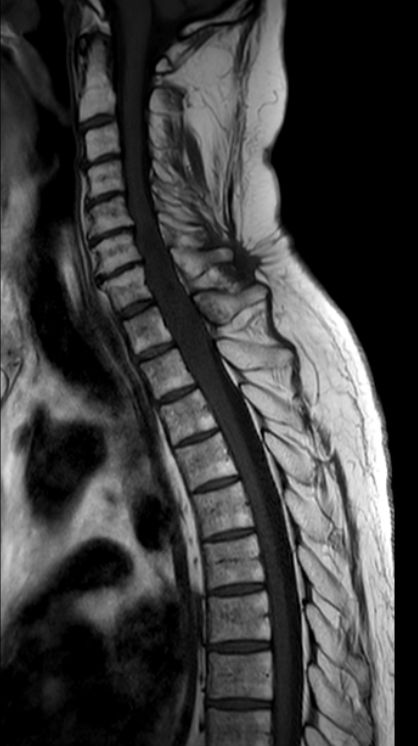 |
MRT T2W-Bild
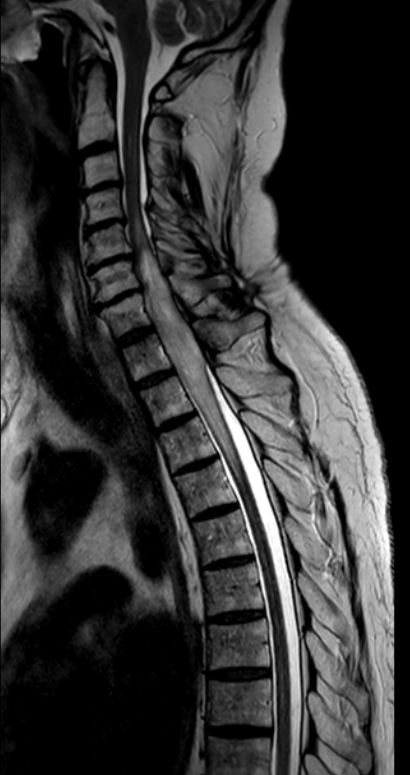 |
MRT T2W-Bild. Hier ist die Degeneration des Myelons unterhalb des Tumors erkennbar.
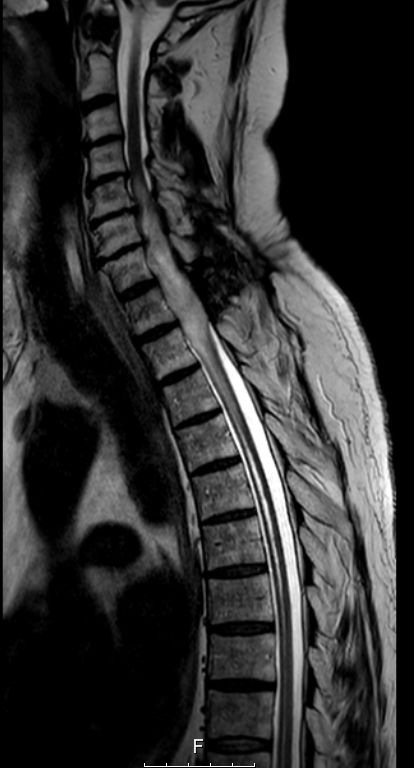 |
| Therapie |
Nach den Ergebnissen der CATNON-Studie ist die beste Primärbehandlung: |
- möglichst radikale Exzision
- postoperative Bestrahlung
- adjuvante Chemotherapie mit Temozolomid
|
| Bestrahlung |
Eine postoperative Bestrahlung verbessert signifikant das Überleben anaplastischer Astrozytome.
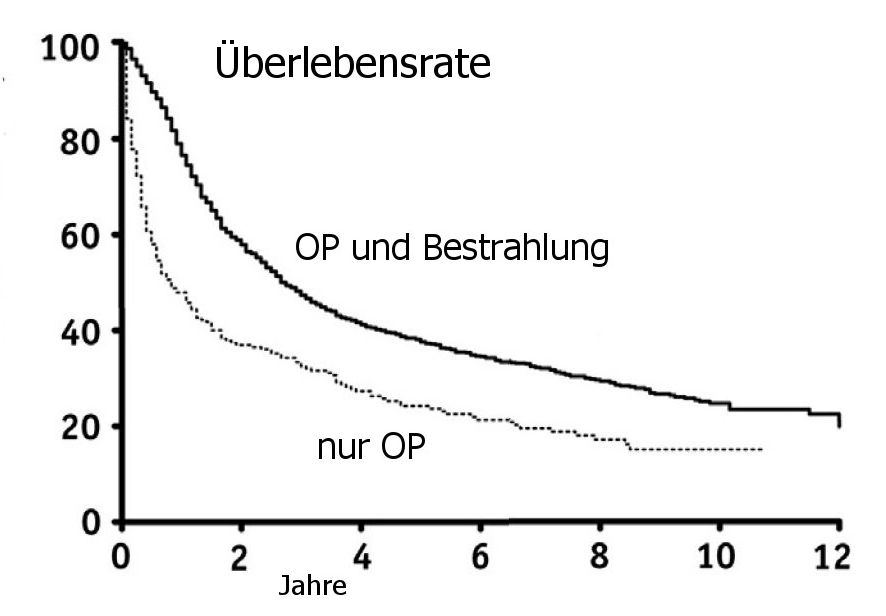
Modifiziert nach (3). SEER-Analyse. |
| Ergebnisse |
|
Der Nutzen einer zusätzlich zur Strahlentherapie erfolgenden Chemotherapie bei neu diagnostizierten Grad-III-Gliomen ohne 1p/19q- Kodeletion ist noch unbekannt.
Die CATNON-Studie (NCT00626990) untersucht den Einfluss adjuvanter und/oder begleitender Chemotherapie mit Temozolomid bei diesen Tumoren.
Patienten mit neu diagnostiziertem Grad-III-Gliom ohne 1p/19q-Kodeletion werden in folgende Studienarme randomisiert:
1) nur Strahlentherapie;
2) Strahlentherapie + begleitende Chemotherapie;
3) Strahlentherapie plus 12 Zyklen adjuvanter Chemotherapie;
4) Strahlentherapie + begleitende und adjuvante Chemotherapie.
Die Daten der Interimanalyse zeigen für die beiden Gruppen mit adjuvanter Chemotherapie
sowohl ein besseres Gesamtüberleben (OS) (HR = 0,645) als auch ein längeres
progressionsfreies Überleben (PFS) (HR = 0,586). Der MGMT-Status konnte bei
74% der Patienten bestimmt werden und weist bei 42% eine Methylierung auf.
Eine MGMT-Methylierung geht mit einer verbesserten Prognose für das
progressionsfreie und das Gesamtüberleben einher (HR = 0,54), war aber zu
diesem Zeitpunkt der Datenauswertung nicht prädiktiv für einen verbesserten
Therapieerfolg bei adjuvanter Chemotherapie mit Temozolomid |
Teil von |
Gliome |
ZNS-Tumore |
Onkologie |
| Quellen |
1.) Stupp R, et al.:
Anaplastic Astrocytomas in adults.
Critical Reviews in oncology/hematology 63(2007):72–80
2.) Reardon D, et al.:
Recent advances in the treatment of malignant astrocytoma.
JCO 2006;24:1253-1265
3.) Rusthoven CG, et al.:
The Impact of Adjuvant Radiation Therapy for High-Grade Gliomas by Histology
in the United States Population.
Int J Radiation Oncol Biol Phys 90(2014): 894-902
|
 |




