- Lunge
- Thymus
- Magen
- Duodenum
- oberes Jejunum
- Pankreas
- unteres Jejunum
- Ileum
- Appendix
- proximales Colon
- Zökum
- distales Colon
- Rektum
- G1 (Karzinoid)
- G2
- G3 (klein- oder großzelliges) neuroendokrines Karzinom
| Name | Leitsymptom | Hormon | Andere Hormone im Tumor | Malignitätsrate | Lokalisation |
| Karzinoid - Syndrom | Durchfälle, Flush, Bronchoobstruktion | Serotonin, Tachykinine | Prostaglandine | 100% | lleumPankreas |
| Insulinom | Nüchternhypoglykämie | Insulin | Glucagon, PP | 5-10% | Pankreas |
| Gastrinom (Zollinger-Ellison- Syndrom) | Säurehypersekretion, rezidivierende Ulzera, Steatorrhoe, Diarrhoe | Gastrin | Insulin, PP, Glucagon, ACTH, Somatostatin | > 90% | Pankreas; selten: Duodenum, Magen, Mesenterium |
| VIPom (Verner-Morrison- Syndrom, pankreatische Cholera) | wäßrige Diarrhoe, Hypokaliämie, Subazidität | VIP, PHI | PP, Glucagon, Somatostatin | 75% | Pankreas; seltener Grenzstrang (Neuroblastom, Ganglioneuroblastom) |
| Glukagonom | nekrolytisches, migratorisches Erythem, Diabetes mellitus, Anämie | Glucagon | PP, Insulin, Somatostatin | 50% | Pankreas |
| Somatostatinom | Diabetes mellitus, Steatorrhoe, Cholelithiasis | Somatostatin | PP, Insulin, Calcitonin | 50% | Pankreas, Duodenum |
| GRFom | Akromegalie | GH-RH | Somatostatin,Gastrin, Insulin, ACTH | 100% | Pankreas, Lunge |
| Funktionell inaktive Tumoren | fehlt, bei großen Tumoren lokale Symptome | Serotonin, Somatostatin, PP, Glucagon | > 90% | Pankreas, Dünndarm, Dickdarm |
- Insulinom
- Gastrinom
- Glugagonom
- VIPom
- Somatostatinom
- pankreatisches Polypeptidom
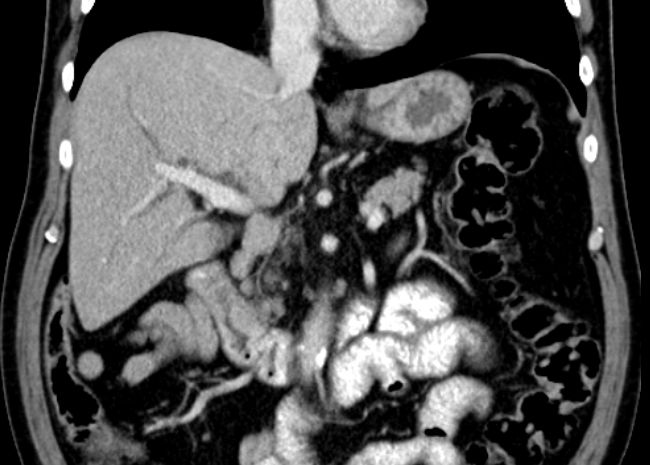
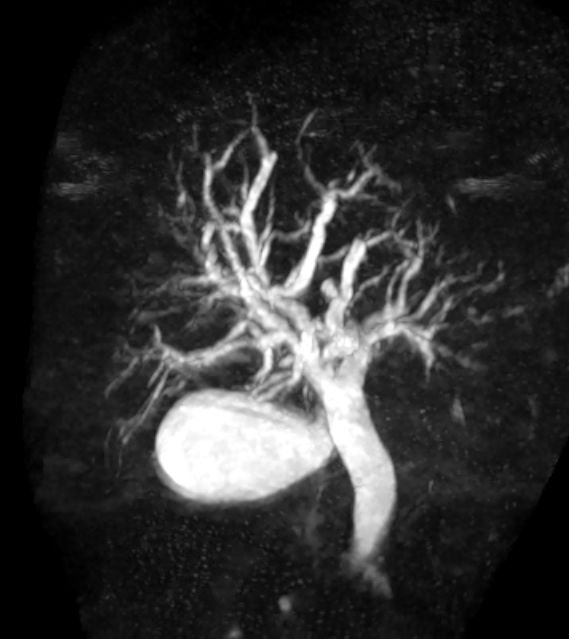
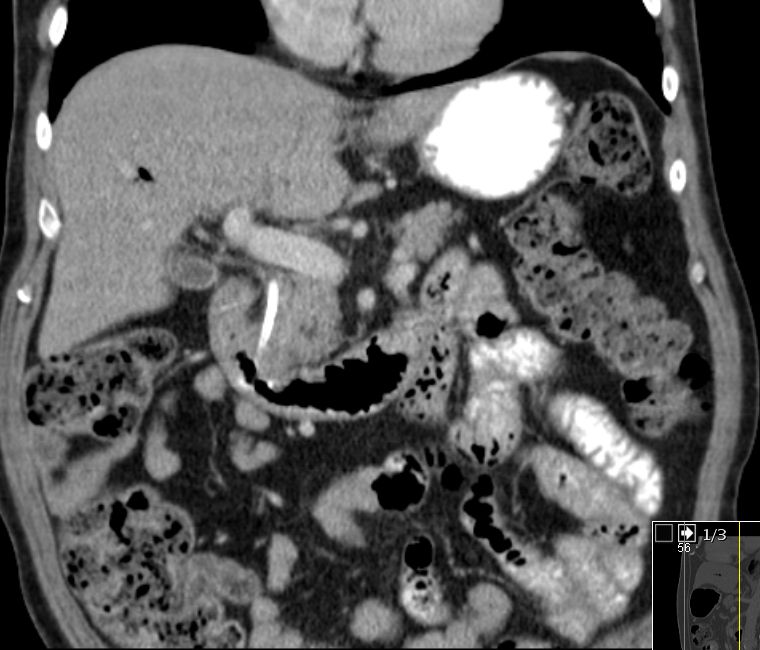
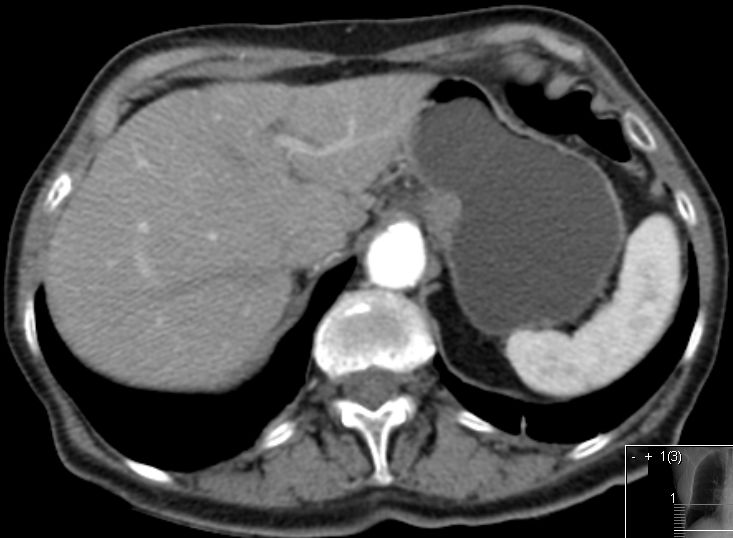
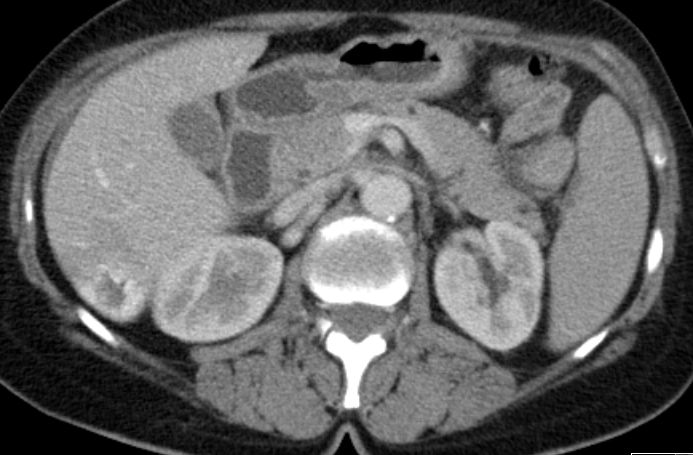
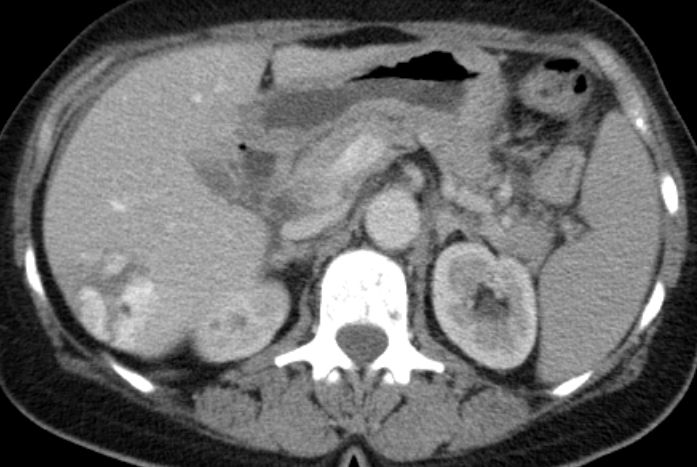
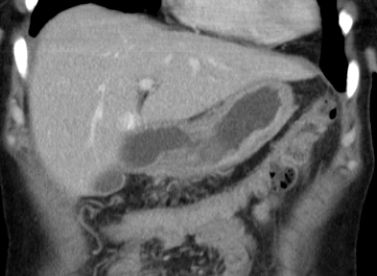
80 cm oral des terminalen Ileum fand sich ein Meckelsches Divertikel mit derbem Inhalt.
Histologisch neuroendokrinen Tumor, G1 (Mitosezahl pro 10 HPF unter 2, Ki 67-Index unter 2 %). Staging: pT1a.
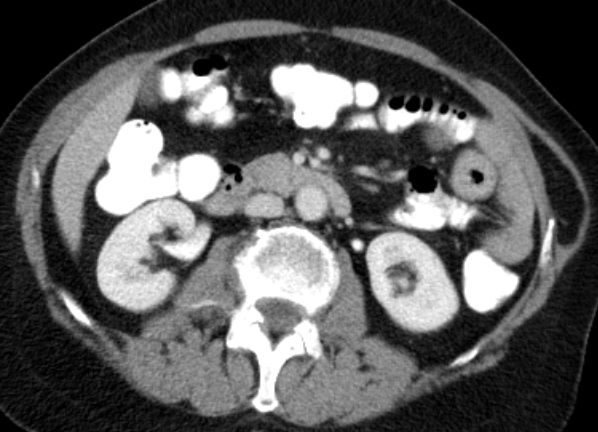
Histologie: gut differenzierter neuroendokriner Tumor, G1, Ki67 unter 1%.
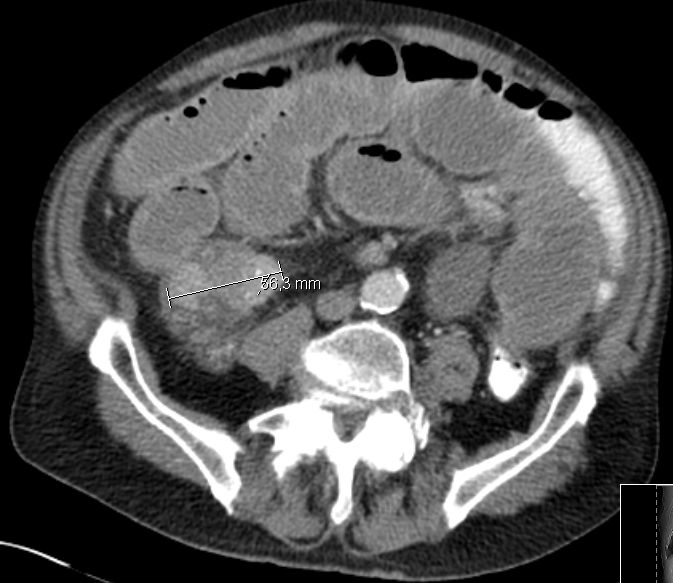
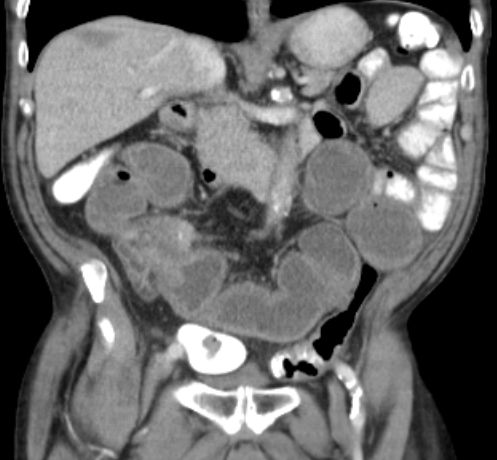
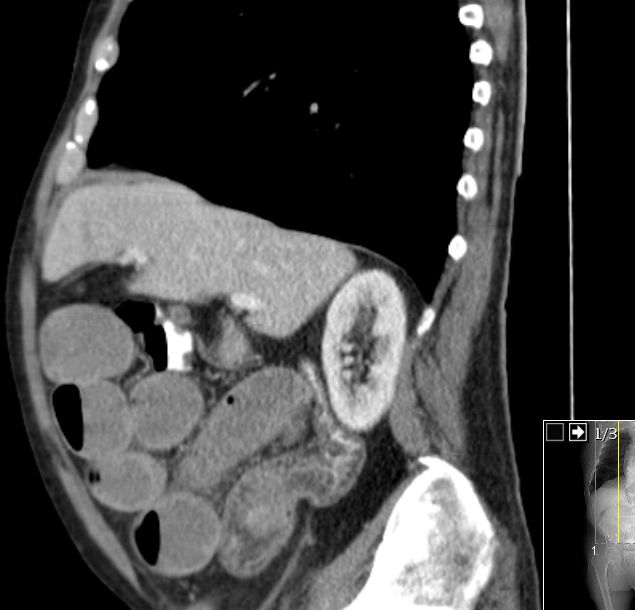
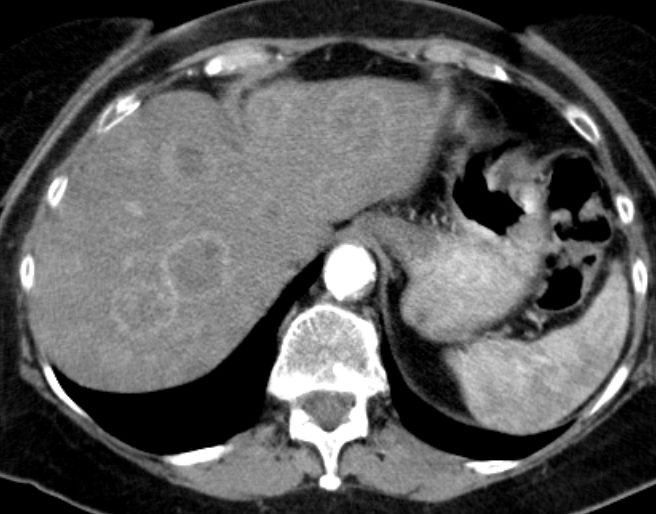
Placebo-controlled, double-blind, prospective, randomized study on the effect of octreotide LAR in the control of tumor growth in patients with metastatic neuroendocrine midgut tumors: a report from the PROMID Study Group.
JCO 27(2009):4656-4663
2.) Williams ED, Sandler M:
The classification of carcinoid tumors.
Lancet 1963; 1: 238–9
3.) Klöppel G, Rindi G, Anlauf M, Perren A, Komminoth P:
Site-specific biology and pathology of gastroenteropancreatic neuroendocrine tumors.
Virchows Arch 2007; 451 Suppl 1: 9–27
4.) Rindi G, Arnold R, Bosman FT, et al.:
Nomenclature and classification of neuroendocrine neoplasms of the digestive system.
In:
Bosman FT, Carneiro F, Hruban RH, Theise ND (eds.):
WHO classification of tumors of the digestive system.
Lyon: IARC 2010.
5.) Rindi G, Klöppel G, Couvelard A, et al.:
TNM staging of midgut and hindgut (neuro) endocrine tumors: a consensus proposal including a grading system.
Virchows Arch 2007; 451: 757–62
6.) Rindi G, Luinetti O, Cornaggia M, Capella C, Solcia E:
Three subtypes of gastric argyrophil carcinoid and the gastric neuroendocrine carcinoma: a clinicopathologic study.
Gastroenterology 1993;104:994–1006
7.)O’Toole D, Grossman A, Gross D, et al.:
ENETS Consensus Guidelines for the Standards of Care in Neuroendocrine Tumors: biochemical markers.
Neuroendocrinology 2009; 90: 194–202
8.) Auernhammer CJ, Spitzweg C, Angele MK, et al.:
Advanced neuroendocrine tumours of the small intestine and pancreas: Clinical developments, controversies, and future strategies.
Lancet Diabetes Endocrinol 2018;6:404-415
Teil von
