zurück
Home |
PD-1-IH, Programmed Cell Death - 1 - Inhibitor |
allgemeines |
Auf der Oberfläche aktivierter T-Zellen befinden sich Rezeptoren,
die bei Aktivierung einen Immunangriff auf körpereigene Zellen verhindern. |
Dieser Mechanismus wird von Tumorzellen missbraucht, um der Immunabwehr zu entgehen. |
Wirkprinzip |
Tumorzellen exprimieren oft PD-1.
Aktivierte T-Zellen binden mit PD-L1 an PD-L. |
Dadurch wird ein Angriff der T-Zellen auf die Tumorzellen verhindert. |
Am wichtigsten sind die CD8--T-Zellen. |
TPS |
Zahl der PD-1-positiven Tumorzellen / Gesamtzahl der Tumorzellen |
Tumormutationen |
Je mehr somatische Mutationen ein Tumor hat, umso höher ist die objektive Ansprechrate bei einer Therapie mit PD-1-Inhibitoren
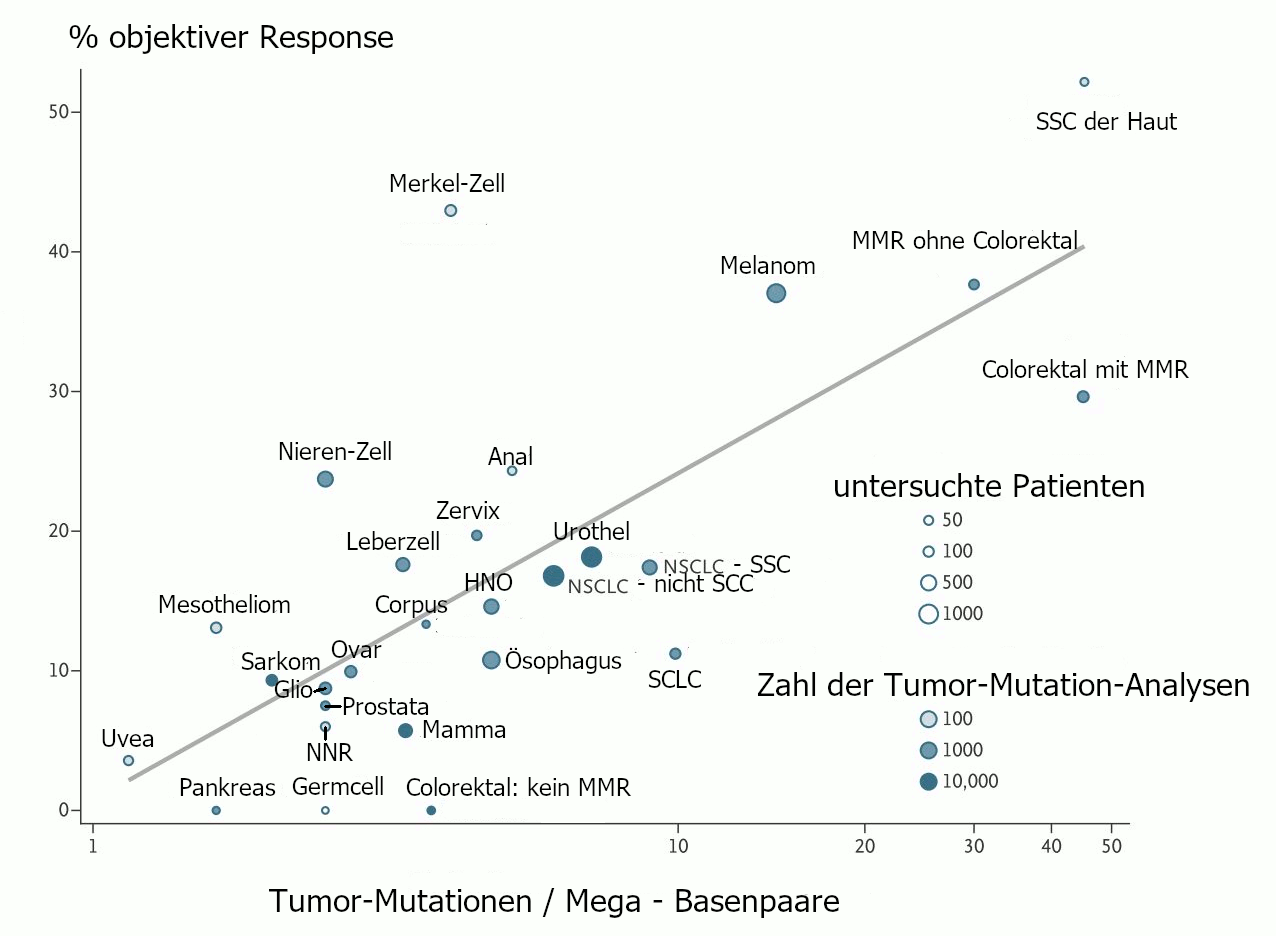
Kein MMR: Mismatch Repair Defizit nicht nachweisbar.
Mit MMR: Mismatch Repair Defizit nachweisbar.
SCC: Plattenepithel - Karzinom.
Nach Daten von (2). |
VENTANA PD-L1 (SP263) Assay |
Prüfung auf PD-L1 - Protein an Formalin-fixierten, Paraffin-eingebetteten Urothelkarzinom-Gewebe. |
| Nivolumab, OPDIVO® |
humaner IgG4-MBA |
bindet an den PD-1 Rezeptor |
Blockiert den Angriff von PD-L1 und PD-L2 |
| Anwendung beim NSCLC in der CheckMate-017 - Studie |
Phase I - Prüfung beim Melanom |
Phase - II - Prüfung beim metastasierten Nierenzellkarzinom. |
| Pembrolizumab, Keytruda® |
Blockiert PD-L1 und PD-L2 |
Zulassung zur Behandlung des fortgeschrittenen, nicht resezierbaren oder metastasierten Melanoms bei Erwachsenen.
NSCLC, Nierenzellkarzinom, HNO-SCC, Colorektales Karzinom |
Rezidiviertes Hodgkin-Lymphom: Phase II |
| Lambrolizumab |
| Atezolizumab TECENTRIQ® |
Blockiert PD-L1 |
NSCLC, second line Phase III |
Phase I - Prüfung beim metastasierten Nierenzellkarzinom |
Urothel-Ca |
| OAK (1) |
Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer. |
| Durvalumab, IMFINZI® |
Blockiert die Bindung von PD-L1 an PD-1 und CD80 |
selectiver, hoch affiner G1 - MBA |
| NSCLC:
PACIFIC-Studie |
Zulassung Urothel - Karzinom
(NIAGARA-Studie)(4):
- fortgeschritten oder
- metastasiert oder
- Progress während oder nach Platin-Chemotherapie oder
- Progress innerhalb von 12 Monaten nach adjuvanter oder praeoperativer Platin-Chemotherapie
|
Zulassung NSCLC:
- Stadium III
- ≥1% PD-L1-positive Tumorzellen
- kein Progress unter Platin-haltiger Radiochemotherapie
|
| Avelumab |
MBA gegen PD-L1 nicht PD-L2 |
Merckel-Zell-Ca |
Metastasiertes Urothel-Ca: JAVELIN Renal 101 (Phase III) |
| Dostarlimab |
JEMPERLI® |
Zulassung
- Endometriumkarzinom
- rezidivierend oder fortgeschritten
- während oder nach Platin-basierter Therapie progredient
- Mismatch-Reparatur-Defizienz (dMMR)/hohe Mikrosatelliteninstabilität (MSI-H)
|
RUBI-Studie |
| Camrelizumab |
|
| Cemiplimab |
Libtayo® |
SCC der Haut(3) |
| Toripalimab, Loqtorzi® |
chinesisches Präparat |
Indikationen: Rezidivierendes oder metastasiertes Nasopharynxkarzinom
Fortgeschrittenes oder metastasiertes Ösophagus‑Plattenepithelkarzinom |
| Sintilimab |
chinesisches Präparat |
| Hautkomplikationen |
Grad 1:
Ausschlag, entzündliche Hautreaktion
Lokale Therapie
Fortsetzung der Behandlung nach Verschwinden der Symptome |
Grad 2:
blasenbildende Hauterscheinung,
Lokale Therapie Ev. Anti-IL-4 (Dupilumab),
Fortsetzung der Behandlung nach Verschwinden der Symptome. |
Grad 3: schwere Hautreaktion (SCAR),
Behandlung sofort stoppen |
Teil von |
Immunmodulatoren |
immunologische Therapie |
Therapie von Tumorerkrankungen |
Onkologie |
| Quellen |
1.) Rittmeyer A Barlesi F, et al.:
Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer (OAK):
a phase 3, open-label, multicentre randomised controlled trial.
Lancet 2017; 389: 255–65.
2.) Yarchoan M, Hopkins A, Jaffee EM, Kimmel S:
Tumor Mutational Burden and Response Rate to PD-1 Inhibition.
NEJM 2017:377:2500-2501
DOI: 10.1056/NEJMc1713444
Comprehensive Cancer Center at Johns Hopkins Baltimore
3.) Migden MR, Khushalani NI, Chang ALS, et al.:
Cemiplimab in locally advanced cutaneous squamous cell carcinoma: Results from an open-label, phase 2, single-arm trial.
Lancet Oncol 2020;21:294-305
4.) Powles T, et al. for the NIAGARA Investigators:
Perioperative Durvalumab with Neoadjuvant Chemotherapy in Operable Bladder Cancer.
N Engl J Med 2024;391:1773-86.
DOI: 10.1056/NEJMoa2408154
|
 |

